- 关于我们
- 服务与能力
- 生产体系
- 哺乳动物细胞
$我们的专业能力覆盖从哺乳动物细胞培养到生物大分子的发现、开发与 cGMP 生产。依托 6 大新药发现平台、一流的 CMC 开发团队以及完善的供应链体系,我们能够为您的生物药开发提供全流程、一体化的解决方案。
- 哺乳动物细胞表达
$从概念到商业化,为您提供哺乳动物细胞生物药开发的一站式全流程服务。
哺乳动物细胞表达
从概念到商业化,为您提供哺乳动物细胞生物药开发的一站式全流程服务。
- 支持的产品类型:
- 单克隆抗体
$探索我们针对该类产品提供的全方位药物研发服务
单克隆抗体
探索我们针对该类产品提供的全方位药物研发服务
- 双特异性及多特异性抗体
$探索我们针对该类产品提供的全方位药物研发服务
双特异性及多特异性抗体
探索我们针对该类产品提供的全方位药物研发服务
- Fc融合蛋白
$探索我们针对该类产品提供的全方位药物研发服务
Fc融合蛋白
探索我们针对该类产品提供的全方位药物研发服务
- 抗体片段
$探索我们针对该类产品提供的全方位药物研发服务
抗体片段
探索我们针对该类产品提供的全方位药物研发服务
- 重组蛋白 / 酶 / 细胞因子
$探索我们针对该类产品提供的全方位药物研发服务
重组蛋白 / 酶 / 细胞因子
探索我们针对该类产品提供的全方位药物研发服务
- 抗体偶联药物(ADC)
$探索我们针对该类产品提供的全方位药物研发服务
抗体偶联药物(ADC)
探索我们针对该类产品提供的全方位药物研发服务
- 病毒样颗粒(VLP)
$探索我们针对该类产品提供的全方位药物研发服务
病毒样颗粒(VLP)
探索我们针对该类产品提供的全方位药物研发服务
- 微生物发酵
$全方位 CMC 开发与 cGMP 生产微生物发酵平台。提供基于大肠杆菌及酵母表达系统的质粒 DNA 与重组蛋白生产服务。
- 微生物发酵
$卓越品质,专为微生物发酵来源生物药提供专家级服务。
微生物发酵
卓越品质,专为微生物发酵来源生物药提供专家级服务。
- 支持的产品类型:
- 抗体片段
$探索我们针对该类产品提供的全方位药物研发服务
抗体片段
探索我们针对该类产品提供的全方位药物研发服务
- 酶
$探索我们针对该类产品提供的全方位药物研发服务
酶
探索我们针对该类产品提供的全方位药物研发服务
- 病毒样颗粒(VLP)
$探索我们针对该类产品提供的全方位药物研发服务
病毒样颗粒(VLP)
探索我们针对该类产品提供的全方位药物研发服务
- 核心能力
- 发现
$涵盖从早期概念至 IND 申报的集成化药物发现平台
- 研究探索
$药明生物提供行业专业知识、最先进的设施和多种抗体生成技术平台,用于发现新型单克隆 双特异性和多特异性抗体、免疫细胞因子和其他生物制剂。
研究探索
药明生物提供行业专业知识、最先进的设施和多种抗体生成技术平台,用于发现新型单克隆 双特异性和多特异性抗体、免疫细胞因子和其他生物制剂。
- 开发
$依托全球规模领先、经验丰富的开发团队,我们拥有卓越的资源、技术与专业实力,致力于以最高效、最具成本效益的方式,驱动您的项目顺利推进至 IND 与 BLA 申报。
- 细胞株工程
$无论是作为独立服务,还是作为我们集成化 CMC 开发平台的一部分,药明生物都能在广泛的生物药领域,为客户提供深厚的专业积淀,以及行业领先的细胞株工程与菌株开发周期。
细胞株工程
无论是作为独立服务,还是作为我们集成化 CMC 开发平台的一部分,药明生物都能在广泛的生物药领域,为客户提供深厚的专业积淀,以及行业领先的细胞株工程与菌株开发周期。
- 细胞株构建
- 分析科学
$我们提供全方位的分析检测服务,在过程控制(IPC)、成品放行及稳定性研究的方法开发领域拥有顶尖的专业实力。此外,我们还支持细胞株构建、工艺及制剂开发、产品表征、可开发性评估,以及其他支持 IND 和 BLA 申报的关键研究。
分析科学
我们提供全方位的分析检测服务,在过程控制(IPC)、成品放行及稳定性研究的方法开发领域拥有顶尖的专业实力。此外,我们还支持细胞株构建、工艺及制剂开发、产品表征、可开发性评估,以及其他支持 IND 和 BLA 申报的关键研究。
- 上下游工艺开发
$我们拥有多个上游与下游工艺开发实验室,支持分批补料、强化分批补料及连续生产工艺的建立与放大。我们的服务涵盖多种生物药类型,贯穿药物研发的早期及后期阶段。
上下游工艺开发
我们拥有多个上游与下游工艺开发实验室,支持分批补料、强化分批补料及连续生产工艺的建立与放大。我们的服务涵盖多种生物药类型,贯穿药物研发的早期及后期阶段。
- 细胞库建库
$我们提供一站式自有细胞库构建与细胞系表征服务,符合全球 GMP 法规及 ICH 指南要求;同时运营超过 20 个 cGMP 级细胞库车间,确保该关键 CMC 开发环节具备充足产能并可按时执行。
细胞库建库
我们提供一站式自有细胞库构建与细胞系表征服务,符合全球 GMP 法规及 ICH 指南要求;同时运营超过 20 个 cGMP 级细胞库车间,确保该关键 CMC 开发环节具备充足产能并可按时执行。
- 生产
$我们在四个国家布局了多座先进且高品质的 cGMP 生产设施,涵盖临床及商业化规模的药物原液(DS)和制剂(DP)生产,能够支持来源于哺乳动物及微生物表达系统的多种生物制品生产。
- 临床原液(DS)GMP生产
$运营多个高质量、先进的临床规模 cGMP 设施,用于生物制药原液(DS)生产,涵盖哺乳动物和微生物两种表达系统。
临床原液(DS)GMP生产
运营多个高质量、先进的临床规模 cGMP 设施,用于生物制药原液(DS)生产,涵盖哺乳动物和微生物两种表达系统。
- 临床制剂(DP)GMP生产
$多个高度灵活的临床规模制剂(DP)生产设施,按照全球监管机构定义的现行药品生产质量管理规范(cGMP)要求,用于生物制剂和注射用制剂的配方、灌装、贴标及包装。
临床制剂(DP)GMP生产
多个高度灵活的临床规模制剂(DP)生产设施,按照全球监管机构定义的现行药品生产质量管理规范(cGMP)要求,用于生物制剂和注射用制剂的配方、灌装、贴标及包装。
- 商业化生产
$药明生物在四个国家拥有多个先进的、高质量的cGMP原液和制剂生产设施。利用多种规格的、经过验证的西林瓶、胶塞和铝盖组合平台,能够在不同的临床阶段和商业化生产规模上进行水针或冻干制剂产品生产。
商业化生产
药明生物在四个国家拥有多个先进的、高质量的cGMP原液和制剂生产设施。利用多种规格的、经过验证的西林瓶、胶塞和铝盖组合平台,能够在不同的临床阶段和商业化生产规模上进行水针或冻干制剂产品生产。
- 药物生产
- 药物cGMP填充和完成
- 检测
$我们在工艺过程检测、产品表征、放行检测及稳定性方法的开发与检测方面具备深厚的专业能力,既可作为一体化生物药开发平台的支持服务提供,也可作为独立项目开展。我们覆盖广泛的分析检测与生物安全检测卓越中心,以及经监管机构批准的质量控制(QC)实验室,是我们为客户提供各项服务的核心支撑。
- 生物药安全检测
$我们拥有符合 EMA、ISO (CNAS) 及 CMA 认证的高质量自有生物安全检测设施,能够为原材料、细胞株及未加工原液提供外源因子筛查,并结合卓越的病毒清除验证能力,为客户提供一站式生物安全检测服务解决方案。
生物药安全检测
我们拥有符合 EMA、ISO (CNAS) 及 CMA 认证的高质量自有生物安全检测设施,能够为原材料、细胞株及未加工原液提供外源因子筛查,并结合卓越的病毒清除验证能力,为客户提供一站式生物安全检测服务解决方案。
- 分析检测
$凭借全方位的检测开发与分析测试能力,我们助力药物研发的全生命周期——从关键表征研究到支持 IND/BLA 申报的各项试验,包括专业的生物分析与法医鉴定。我们致力于为您独特的产品需求提供量身定制的定制化方案。
分析检测
凭借全方位的检测开发与分析测试能力,我们助力药物研发的全生命周期——从关键表征研究到支持 IND/BLA 申报的各项试验,包括专业的生物分析与法医鉴定。我们致力于为您独特的产品需求提供量身定制的定制化方案。
- 卓越中心
$我们的卓越中心(CoE)在产品全生命周期内提供专业的检测支持,旨在加速项目进程,并确保项目在商业化阶段具备完善的分析就绪能力。
卓越中心
我们的卓越中心(CoE)在产品全生命周期内提供专业的检测支持,旨在加速项目进程,并确保项目在商业化阶段具备完善的分析就绪能力。
- 质量标准
- 质量管理
$我们拥有世界一流的质量体系,并在全球各生产基地实现统一标准化管理。我们的质量体系已通过包括美国 FDA、欧洲 EMA、中国 NMPA、日本 PMDA、韩国 MFDS、新加坡 HSA、巴西 ANVISA 及加拿大卫生部(Health Canada)在内的多家全球监管机构认证,支持多种生物药品的生产与检测。
- 全球质量合规部(GQC)
$我们的全球质量与合规团队统筹审计、IT 质量及风险管控,将合规意识贯彻至每一个环节。这确保了我们交付的每一件生物制品都拥有卓越的安全性与疗效,并在执行标准上与您的要求高度对齐。
全球质量合规部(GQC)
我们的全球质量与合规团队统筹审计、IT 质量及风险管控,将合规意识贯彻至每一个环节。这确保了我们交付的每一件生物制品都拥有卓越的安全性与疗效,并在执行标准上与您的要求高度对齐。
- 质量保证
$全球合规体系、全员质量承诺。依托全球生产基地统一的 QA 标准,我们为生物药及疫苗的商业化生产提供稳定、可靠、符合国际主流监管要求的质量支撑。
质量保证
全球合规体系、全员质量承诺。依托全球生产基地统一的 QA 标准,我们为生物药及疫苗的商业化生产提供稳定、可靠、符合国际主流监管要求的质量支撑。
- 质量控制
$我们拥有符合法规要求的自有 QC 实验室,为所有临床及商业化 GMP 生产基地提供全流程支持。我们不仅确保生产前后的产品高质量检测,更对环境监测、清洗验证、仪器生命周期管理、样品/留样管理及审计等关键职能进行全面监督。
质量控制
我们拥有符合法规要求的自有 QC 实验室,为所有临床及商业化 GMP 生产基地提供全流程支持。我们不仅确保生产前后的产品高质量检测,更对环境监测、清洗验证、仪器生命周期管理、样品/留样管理及审计等关键职能进行全面监督。
- 法规事务
$依托深厚的法规专业积淀,我们为客户提供从 CMC 申报资料、药物递交到药物注册的全方位支持。自 2015 年起,我们已成功支持全球客户申报超过550 余项 IND、CTA、BLA、MAA、NDA 及 EUA 申报,完成200 多个 Module 3 CMC 申报件。
法规事务
依托深厚的法规专业积淀,我们为客户提供从 CMC 申报资料、药物递交到药物注册的全方位支持。自 2015 年起,我们已成功支持全球客户申报超过550 余项 IND、CTA、BLA、MAA、NDA 及 EUA 申报,完成200 多个 Module 3 CMC 申报件。
- 技术平台
- 发现
$药明生物提供了先进全面的抗体发现服务,用于创新型抗体的发现、鉴定和筛选提供全方位的服务。
- WuXiBody ® 双特异性抗体平台
$WuXiBody ® 平台是药明生物开发的一个创新的、专有的技术平台,用于扩大双特异性抗体应用范围。基于最新的工程设计,该平台可以加快6-18个月的研发进程,大幅度降低产品的成本。
WuXiBody ® 双特异性抗体平台
WuXiBody ® 平台是药明生物开发的一个创新的、专有的技术平台,用于扩大双特异性抗体应用范围。基于最新的工程设计,该平台可以加快6-18个月的研发进程,大幅度降低产品的成本。
- WuXiHYbrid™ 杂交瘤单克隆抗体研发平台
$WuXiHYbrid™ 是国内领先、世界一流杂交瘤抗体研发平台,突破性提高了抗体新药研发的质量和速度,已为国内外50+客户成功交付超过200个高质量的单克隆抗体研发项目。
WuXiHYbrid™ 杂交瘤单克隆抗体研发平台
WuXiHYbrid™ 是国内领先、世界一流杂交瘤抗体研发平台,突破性提高了抗体新药研发的质量和速度,已为国内外50+客户成功交付超过200个高质量的单克隆抗体研发项目。
- WuXiLiAb™ 噬菌体展示人抗体库
$全人天然抗体库选取60个健康供体, 总数大于6x10e9 的PBMC或CBMC, 每个供体都单独建库并系统QC,保证了文库的高质量和多样性。
WuXiLiAb™ 噬菌体展示人抗体库
全人天然抗体库选取60个健康供体, 总数大于6x10e9 的PBMC或CBMC, 每个供体都单独建库并系统QC,保证了文库的高质量和多样性。
- 开发
$前沿的生物工艺平台与技术,旨在以更快的速度、更高的效率和更具成本效益的方式,推动高质量生物制剂进入临床试验阶段。
- WuXian™ 定制化蛋白生产服务
$依托药明生物行业领先的高通量高表达、纯化和分析技术,提供各类蛋白生产服务,其中包括抗体、双抗、酶和重组蛋白表达。
WuXian™ 定制化蛋白生产服务
依托药明生物行业领先的高通量高表达、纯化和分析技术,提供各类蛋白生产服务,其中包括抗体、双抗、酶和重组蛋白表达。
- WuXia™ 细胞株构建
$药明生物为多种生物治疗药物提供全面的哺乳动物细胞系开发服务,从客户提供的DNA或蛋白质序列开始,到交付出高产量、高产品质量且稳定的单克隆结束。
WuXia™ 细胞株构建
药明生物为多种生物治疗药物提供全面的哺乳动物细胞系开发服务,从客户提供的DNA或蛋白质序列开始,到交付出高产量、高产品质量且稳定的单克隆结束。
- WuXiUPTM 超高效连续细胞培养生产平台
$WuXiUPTM 平台是强化型的灌流工艺,提供高产量,高质量的新一代生物药制造解决方案,灵活性高,成本低。
WuXiUPTM 超高效连续细胞培养生产平台
WuXiUPTM 平台是强化型的灌流工艺,提供高产量,高质量的新一代生物药制造解决方案,灵活性高,成本低。
- WuXiDARx™偶联技术平台
$药明合联研发了WuXiDARx™技术*,一种基于抗体天然半胱氨酸残基的偶联方式,为生物偶联药管线开发提供了更高的灵活性。
WuXiDARx™偶联技术平台
药明合联研发了WuXiDARx™技术*,一种基于抗体天然半胱氨酸残基的偶联方式,为生物偶联药管线开发提供了更高的灵活性。
- 生产
$先进的生物制造平台赋能全球医疗合作伙伴,助力生物药快速迈向临床并成功上市,造福全球患者。
- 一次性生物反应器
$我们运营着全球规模领先的数个一次性生物反应器生产基地。依托一次性使用系统在降低风险、生产灵活性、成本效益及环境友好性方面的卓越优势,为客户提供高效的生物药生产保障。
一次性生物反应器
我们运营着全球规模领先的数个一次性生物反应器生产基地。依托一次性使用系统在降低风险、生产灵活性、成本效益及环境友好性方面的卓越优势,为客户提供高效的生物药生产保障。
- Scale-Out生物药生产
$通过使用多个同等规模的反应器进行并联生产,我们能有效降低工艺放大风险,为您在临床至上市的各阶段提供极高的生产弹性,确保稳定供应。
Scale-Out生物药生产
通过使用多个同等规模的反应器进行并联生产,我们能有效降低工艺放大风险,为您在临床至上市的各阶段提供极高的生产弹性,确保稳定供应。
- 机器人无菌灌装
$我们采用全程序化、机器人自动化且无手套的隔离器技术,显著降低先进无菌制剂灌装过程中的生产风险。该系统具备极高的灵活性,能够支持各种复杂生物药及多样化包材系统的灌装需求。
机器人无菌灌装
我们采用全程序化、机器人自动化且无手套的隔离器技术,显著降低先进无菌制剂灌装过程中的生产风险。该系统具备极高的灵活性,能够支持各种复杂生物药及多样化包材系统的灌装需求。
- 连续细胞培养生产工艺
$结合强化灌流培养(IPC)与连续直接产物捕获(CDPC),并配备先进设备,实现生产效率提升并降低成本。
- Scale-Out生物药生产
WuXia™ 细胞株构建
广受全球监管机构认可的成熟高产细胞株构建平台

药明生物为各种生物治疗药物提供全面的哺乳动物细胞株构建(CLD)能力,这既是一项独立服务,也是我们一体化CMC(化学、生产和控制)生物药开发平台的一部分。药明生物从客户提供的DNA或氨基酸序列开始,利用WuXia™细胞株构建平台(其中包括高度优化的宿主细胞株和专有载体)为后续工艺开发和GMP生产活动提供高产量(在分批补料模式下高达11 g/L)、高质量且稳定的细胞株。时至今日,我们采用经过严格审查的CLD技术和工艺构建了超过900个稳定的细胞株,用于临床和商业生产。
WuXia™ CLD平台性能概述

我们的CLD平台灵活强大,可生产多种类型的生物药。

从DNA到GMP生产的理想解决方案
WuXia™细胞株构建系统采用专有的CHO-K1细胞株,该细胞株已被证明能够在更短的时间内达到等于或优于行业标准的产量。为促进交付高产量、高质量且稳定的单克隆,所有细胞株构建服务均得到细胞培养工艺开发团队和分析开发团队以及自动化高通量系统的大力支持。除了CHO-K1细胞株,HEK293、WuXiaADCC PLUS™以及CHO-K1 GSKO宿主也可用于不同需求的细胞株构建。
无瑕(WuXia)的英文翻译为 Flawless or Ideal,即“完美无瑕或十分理想”,
这就是我们选择将我们的细胞株构建(CLD)平台命名为 “WuXia”的原因。
如下图所示,WuXia™平台可加速CLD进程,同时具备高产量、高质量和优异的稳定性,从而助力合作伙伴迅速完成IND申报。 WuXiaTM 细胞株构建平台:灵活的时间选择
WuXiaTM 细胞株构建平台:灵活的时间选择 细胞株构建的典型工作流程如下所示 (点击此处查看更详细的流程说明):
细胞株构建的典型工作流程如下所示 (点击此处查看更详细的流程说明):
关键特点:
了解药明生物CLD平台的关键特点,并了解是什么让我们的系统成为生物药开发和最终GMP生产的“理想选择”。
专有的计算机模拟工具箱 – 元数据密码子优化
我们提供一系列用于评估、设计和优化计算机模拟蛋白质分子的工具,其中包括序列倾向和信号肽分析,以及翻译后修饰、免疫原性和聚集预测。
实验室数字化和自动化保证开发质量
药明生物细胞株构建团队在整个细胞株构建流程中使用了多种高通量自动化设备和系统。实验室数字化系统(例如LDMS)和自动化功能具有稳健且可重复的样品处理和加工能力,有助于保证细胞株和产品的质量。
优良的稳定性
WuXia™ CHO-K1平台为大规模商业化生产提供高度稳定的克隆。我们对300多种用于临床和商业生产的生产细胞株进行了细胞株和产品稳定性研究,结果证明我们的宿主细胞株具有一贯的稳健性。
研究人员在使用靶向抗体免疫治疗方法时,往往都会努力实现一个重要机制,即增强抗体依赖性细胞介导细胞毒性(ADCC)的反应。开发新型癌症疗法需要对抗体进行设计和工程化改造,提高ADCC的反应能力,这一方法已被证实可以提高疗效并改善患者预后。
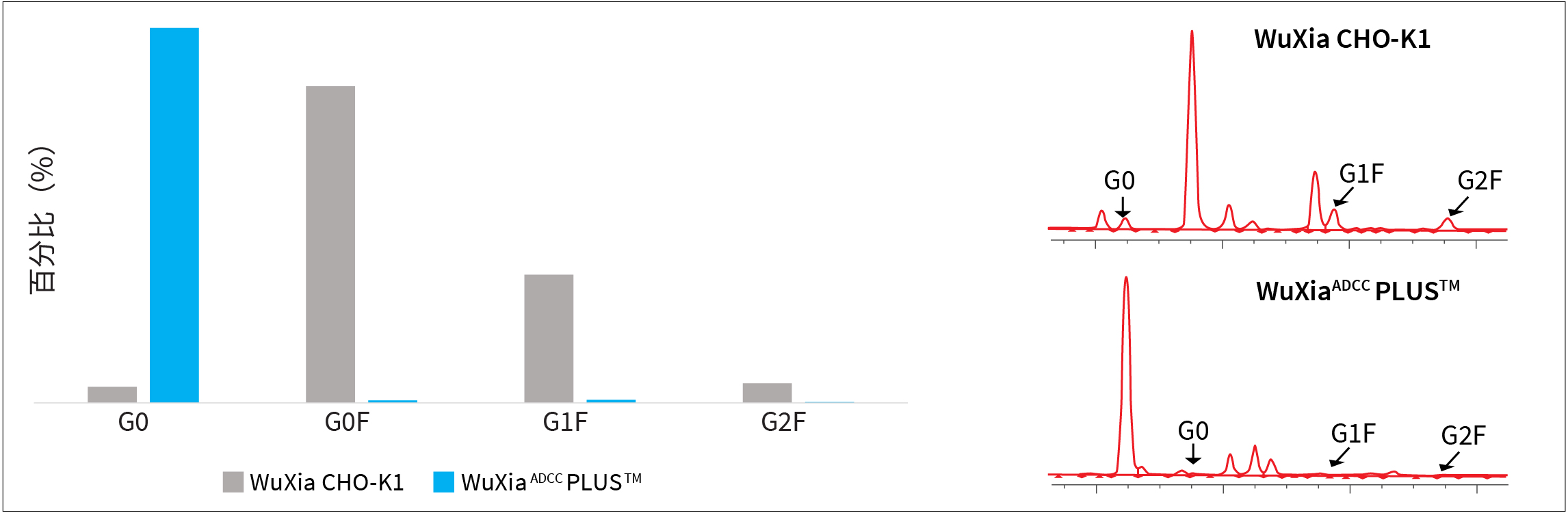
去除N-糖基化位点上的岩藻糖是增强ADCC活性和提高抗体免疫疗法效力的一种高效且经济实惠的方法。为了满足全球对去岩藻糖基化抗体不断增长的需求,我们开发出WuXiaADCC PLUS™细胞株。WuXiaADCC PLUS源自药明生物经过严格审查的WuXia™ CHO-K1细胞株,因此,前者表现出与WuXia CHO-K1亲代细胞株相当的强劲生长能力和代谢特性。
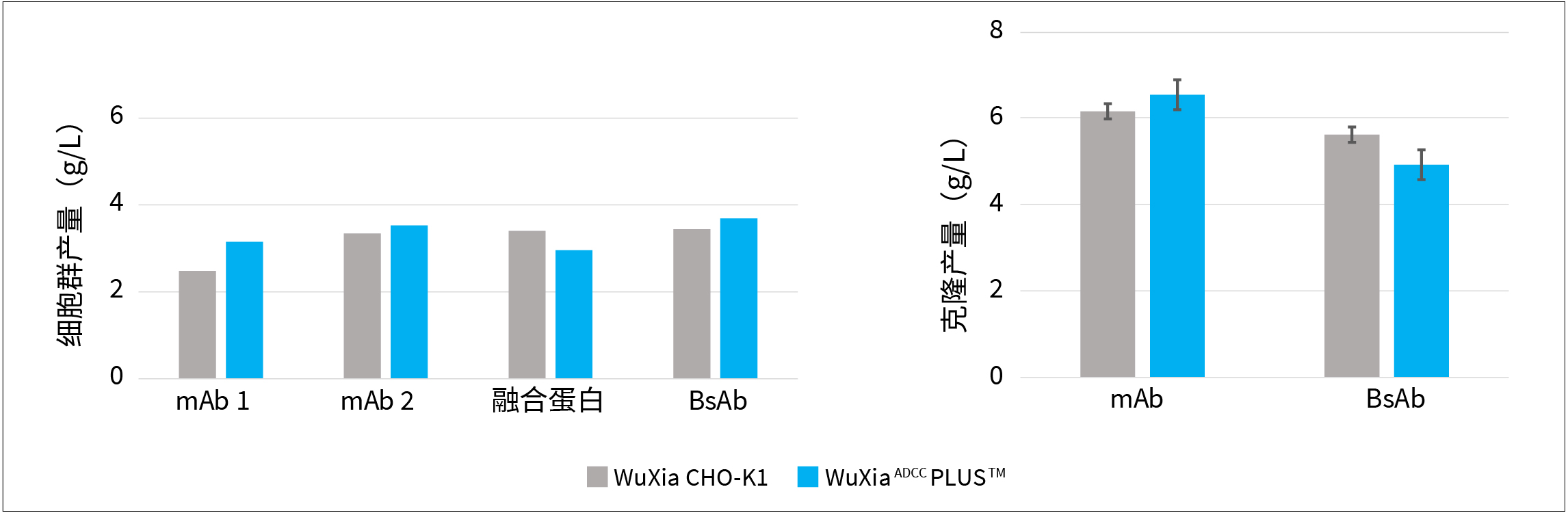
图1表明,WuXiaADCC PLUS细胞株生产的去岩藻糖基化抗体展现出显著增强的ADCC活性
WuXiaADCC PLUS的平均mAb克隆产量为6 g/L,同时还兼容WuXia细胞培养平台工艺,可稳定生产各种规模的去盐藻糖基化抗体,以便用于临床和商业生产。
配套服务
以下功能既可作为我们一体化细胞株构建活动的一部分,也可作为我们提供的独立服务。
为分析项目提供支持的试剂和生物测定细胞株
除生物药细胞株构建服务外,药明生物的CLD团队还生成用于蛋白质试剂生产的细胞株和生物测定细胞株,为整个构建过程和GMP质量控制测试中的分析项目提供支持。
如需了解更多信息,请点击此处。
专业化二代测序和分子生物学服务
药明生物提供多种用于评估细胞株和相关基因的二代测序方法和其他关键分子生物学方法。这些方法既可为一体化细胞株构建项目提供支持,也可作为一项独立服务。 如需了解更多信息, 请点击此处
在可开发性研究和细胞构建活动中,我们提供广泛且全面的分析方法来评估产品。我们的分析服务可为CLD提供支持,其中包括:
- 纯度
- 聚合度
- 同一性
- 产量
- 聚糖图谱
- 结合或效价试验
- 电荷差异
- 序列方差
- 翻译后修饰
我们的计算机模拟评估工具箱专为客户评估多个先导分子候选药物设计,以便客户做出经济、高效的CMC产品开发决策。这种计算机模拟分析可以预测并降低可生产性、稳定性、免疫原性以及其他问题引起的后续开发问题风险,此外,该分析服务还可以整合到CLD项目中,也可以作为定制的独立服务提供给客户。
我们的计算机模拟评估包含三个核心方面:
- 序列分析
- 聚合倾向
- 免疫原性测定
进行序列分析时,我们首先检查序列元素,确定未知结构域/基序,然后验证是否存在可能易受化学和酶修饰影响的序列区域(“热点”)。
对于聚合倾向,我们会根据蛋白质的表面疏水性、电荷和游离半胱氨酸残基来计算聚合概率。
最后,我们会计算序列与MHC分子结合的可能性,并比较序列与人类BCR数据库的相似性,从而评估该分子的免疫原性风险。
通过计算机模拟评估,可以在下一步开发中剔除CMC风险较高的分子候选药物,节省成本并确保满足开发时间进程。下面是我们计算机模拟生物分子评估项目的典型数据或分析结果。
一站式创建细胞库
药明生物提供获得EMA、PMDA和NMPA认证的全面、一站式细胞建库服务。我们拥有22个cGMP细胞库车间,每年可生产超过440个主细胞库(MCB)、工作细胞库(WCB)和生产终末细胞库(EOPC)。我们根据全球监管指南(例如ICH、美国FDA、EMA和NMPA)提供内部细胞株构建、细胞株表征和生物安全测试服务并对其进行整合,提供涵盖细胞株工程和GMP 生产细胞库放行的一站式服务,简约高效。
药明生物的生物安全测试实验室在亚太地区(APAC)处于行业领先地位。我们提供的方法不仅全面而且经过验证,符合全球监管指南(例如USP/EP/JP/ChP和ICH、美国FDA、EMA以及NMPA)。提供的服务包括:
- 细胞株表征(PCB/MCB/WCB/EOPC)
- 针对各种生物药以及细胞和基因治疗的支原体、一般病毒和外来病毒检测。
- 针对IND和BLA的病毒清除验证研究。
- 临床和商业未处理收获液(UPB)批次放行服务。
如需获取有关生物安全测试的更多信息,请点击此处。
全球监管机构要求对用于生物药生产的克隆细胞株进行遗传稳定性评估,这些细胞株具有多个染色体插入的表达构建体。它们给出的建议包括通过cDNA定向测序、Southern和/或Northern印迹法来验证核苷酸序列,以及通过qPCR或ddPCR等其他可能的标准来测定拷贝数。
我们提供全面的一站式遗传稳定性评估服务,评估范围涵盖主细胞库(MCB)、工作细胞库(WCB)和生产终末细胞(EOPC),这些评估既可以整合到细胞株构建项目中,也可以作为定制的独立服务提供。我们的分子生物学团队已成功为全球客户完成了140多项IND申报和40多项BLA申请的遗传稳定性研究。
- WuXia™ 细胞株构建
- WuXiHYbrid™ 杂交瘤单克隆抗体研发平台
- WuXiBody ® 双特异性抗体平台
- 质量保证
- 全球质量合规部(GQC)
- 分析检测
- 临床制剂(DP)GMP生产
- 开发
- 研究探索
- 哺乳动物细胞表达
- 哺乳动物细胞
- 生产体系
WuXi Biologics
Offering End-to-End Solutions
- 关于我们
- 服务与能力
- 生产体系
- 哺乳动物细胞
$我们的专业能力覆盖从哺乳动物细胞培养到生物大分子的发现、开发与 cGMP 生产。依托 6 大新药发现平台、一流的 CMC 开发团队以及完善的供应链体系,我们能够为您的生物药开发提供全流程、一体化的解决方案。

- 返回
- 哺乳动物细胞表达
$从概念到商业化,为您提供哺乳动物细胞生物药开发的一站式全流程服务。
哺乳动物细胞表达
从概念到商业化,为您提供哺乳动物细胞生物药开发的一站式全流程服务。
- 支持的产品类型:
- 单克隆抗体
$探索我们针对该类产品提供的全方位药物研发服务
单克隆抗体
探索我们针对该类产品提供的全方位药物研发服务
- 双特异性及多特异性抗体
$探索我们针对该类产品提供的全方位药物研发服务
双特异性及多特异性抗体
探索我们针对该类产品提供的全方位药物研发服务
- Fc融合蛋白
$探索我们针对该类产品提供的全方位药物研发服务
Fc融合蛋白
探索我们针对该类产品提供的全方位药物研发服务
- 抗体片段
$探索我们针对该类产品提供的全方位药物研发服务
抗体片段
探索我们针对该类产品提供的全方位药物研发服务
- 重组蛋白 / 酶 / 细胞因子
$探索我们针对该类产品提供的全方位药物研发服务
重组蛋白 / 酶 / 细胞因子
探索我们针对该类产品提供的全方位药物研发服务
- 抗体偶联药物(ADC)
$探索我们针对该类产品提供的全方位药物研发服务
- 微生物发酵
$全方位 CMC 开发与 cGMP 生产微生物发酵平台。提供基于大肠杆菌及酵母表达系统的质粒 DNA 与重组蛋白生产服务。

- 返回
- 微生物发酵
$卓越品质,专为微生物发酵来源生物药提供专家级服务。
微生物发酵
卓越品质,专为微生物发酵来源生物药提供专家级服务。
- 支持的产品类型:
- 抗体片段
$探索我们针对该类产品提供的全方位药物研发服务
抗体片段
探索我们针对该类产品提供的全方位药物研发服务
- 酶
$探索我们针对该类产品提供的全方位药物研发服务
- 核心能力
- 发现
$涵盖从早期概念至 IND 申报的集成化药物发现平台

- 开发
$依托全球规模领先、经验丰富的开发团队,我们拥有卓越的资源、技术与专业实力,致力于以最高效、最具成本效益的方式,驱动您的项目顺利推进至 IND 与 BLA 申报。

- 返回
- 细胞株工程
$无论是作为独立服务,还是作为我们集成化 CMC 开发平台的一部分,药明生物都能在广泛的生物药领域,为客户提供深厚的专业积淀,以及行业领先的细胞株工程与菌株开发周期。
- 细胞株构建
- 分析科学
$我们提供全方位的分析检测服务,在过程控制(IPC)、成品放行及稳定性研究的方法开发领域拥有顶尖的专业实力。此外,我们还支持细胞株构建、工艺及制剂开发、产品表征、可开发性评估,以及其他支持 IND 和 BLA 申报的关键研究。
分析科学
我们提供全方位的分析检测服务,在过程控制(IPC)、成品放行及稳定性研究的方法开发领域拥有顶尖的专业实力。此外,我们还支持细胞株构建、工艺及制剂开发、产品表征、可开发性评估,以及其他支持 IND 和 BLA 申报的关键研究。
- 上下游工艺开发
$我们拥有多个上游与下游工艺开发实验室,支持分批补料、强化分批补料及连续生产工艺的建立与放大。我们的服务涵盖多种生物药类型,贯穿药物研发的早期及后期阶段。
上下游工艺开发
我们拥有多个上游与下游工艺开发实验室,支持分批补料、强化分批补料及连续生产工艺的建立与放大。我们的服务涵盖多种生物药类型,贯穿药物研发的早期及后期阶段。
- 细胞库建库
$我们提供一站式自有细胞库构建与细胞系表征服务,符合全球 GMP 法规及 ICH 指南要求;同时运营超过 20 个 cGMP 级细胞库车间,确保该关键 CMC 开发环节具备充足产能并可按时执行。
细胞库建库
我们提供一站式自有细胞库构建与细胞系表征服务,符合全球 GMP 法规及 ICH 指南要求;同时运营超过 20 个 cGMP 级细胞库车间,确保该关键 CMC 开发环节具备充足产能并可按时执行。
- 生产
$我们在四个国家布局了多座先进且高品质的 cGMP 生产设施,涵盖临床及商业化规模的药物原液(DS)和制剂(DP)生产,能够支持来源于哺乳动物及微生物表达系统的多种生物制品生产。

- 返回
- 临床原液(DS)GMP生产
$运营多个高质量、先进的临床规模 cGMP 设施,用于生物制药原液(DS)生产,涵盖哺乳动物和微生物两种表达系统。
临床原液(DS)GMP生产
运营多个高质量、先进的临床规模 cGMP 设施,用于生物制药原液(DS)生产,涵盖哺乳动物和微生物两种表达系统。
- 临床制剂(DP)GMP生产
$多个高度灵活的临床规模制剂(DP)生产设施,按照全球监管机构定义的现行药品生产质量管理规范(cGMP)要求,用于生物制剂和注射用制剂的配方、灌装、贴标及包装。
临床制剂(DP)GMP生产
多个高度灵活的临床规模制剂(DP)生产设施,按照全球监管机构定义的现行药品生产质量管理规范(cGMP)要求,用于生物制剂和注射用制剂的配方、灌装、贴标及包装。
- 商业化生产
$药明生物在四个国家拥有多个先进的、高质量的cGMP原液和制剂生产设施。利用多种规格的、经过验证的西林瓶、胶塞和铝盖组合平台,能够在不同的临床阶段和商业化生产规模上进行水针或冻干制剂产品生产。
商业化生产
药明生物在四个国家拥有多个先进的、高质量的cGMP原液和制剂生产设施。利用多种规格的、经过验证的西林瓶、胶塞和铝盖组合平台,能够在不同的临床阶段和商业化生产规模上进行水针或冻干制剂产品生产。
- 药物生产
- 药物cGMP填充和完成
- 临床制剂(DP)GMP生产
- 检测
$我们在工艺过程检测、产品表征、放行检测及稳定性方法的开发与检测方面具备深厚的专业能力,既可作为一体化生物药开发平台的支持服务提供,也可作为独立项目开展。我们覆盖广泛的分析检测与生物安全检测卓越中心,以及经监管机构批准的质量控制(QC)实验室,是我们为客户提供各项服务的核心支撑。

- 返回
- 生物药安全检测
$我们拥有符合 EMA、ISO (CNAS) 及 CMA 认证的高质量自有生物安全检测设施,能够为原材料、细胞株及未加工原液提供外源因子筛查,并结合卓越的病毒清除验证能力,为客户提供一站式生物安全检测服务解决方案。
生物药安全检测
我们拥有符合 EMA、ISO (CNAS) 及 CMA 认证的高质量自有生物安全检测设施,能够为原材料、细胞株及未加工原液提供外源因子筛查,并结合卓越的病毒清除验证能力,为客户提供一站式生物安全检测服务解决方案。
- 分析检测
$凭借全方位的检测开发与分析测试能力,我们助力药物研发的全生命周期——从关键表征研究到支持 IND/BLA 申报的各项试验,包括专业的生物分析与法医鉴定。我们致力于为您独特的产品需求提供量身定制的定制化方案。
分析检测
凭借全方位的检测开发与分析测试能力,我们助力药物研发的全生命周期——从关键表征研究到支持 IND/BLA 申报的各项试验,包括专业的生物分析与法医鉴定。我们致力于为您独特的产品需求提供量身定制的定制化方案。
- 卓越中心
$我们的卓越中心(CoE)在产品全生命周期内提供专业的检测支持,旨在加速项目进程,并确保项目在商业化阶段具备完善的分析就绪能力。
- 质量标准
- 质量管理
$我们拥有世界一流的质量体系,并在全球各生产基地实现统一标准化管理。我们的质量体系已通过包括美国 FDA、欧洲 EMA、中国 NMPA、日本 PMDA、韩国 MFDS、新加坡 HSA、巴西 ANVISA 及加拿大卫生部(Health Canada)在内的多家全球监管机构认证,支持多种生物药品的生产与检测。

- 返回
- 全球质量合规部(GQC)
$我们的全球质量与合规团队统筹审计、IT 质量及风险管控,将合规意识贯彻至每一个环节。这确保了我们交付的每一件生物制品都拥有卓越的安全性与疗效,并在执行标准上与您的要求高度对齐。
全球质量合规部(GQC)
我们的全球质量与合规团队统筹审计、IT 质量及风险管控,将合规意识贯彻至每一个环节。这确保了我们交付的每一件生物制品都拥有卓越的安全性与疗效,并在执行标准上与您的要求高度对齐。
- 质量保证
$全球合规体系、全员质量承诺。依托全球生产基地统一的 QA 标准,我们为生物药及疫苗的商业化生产提供稳定、可靠、符合国际主流监管要求的质量支撑。
质量保证
全球合规体系、全员质量承诺。依托全球生产基地统一的 QA 标准,我们为生物药及疫苗的商业化生产提供稳定、可靠、符合国际主流监管要求的质量支撑。
- 质量控制
$我们拥有符合法规要求的自有 QC 实验室,为所有临床及商业化 GMP 生产基地提供全流程支持。我们不仅确保生产前后的产品高质量检测,更对环境监测、清洗验证、仪器生命周期管理、样品/留样管理及审计等关键职能进行全面监督。
质量控制
我们拥有符合法规要求的自有 QC 实验室,为所有临床及商业化 GMP 生产基地提供全流程支持。我们不仅确保生产前后的产品高质量检测,更对环境监测、清洗验证、仪器生命周期管理、样品/留样管理及审计等关键职能进行全面监督。
- 法规事务
$依托深厚的法规专业积淀,我们为客户提供从 CMC 申报资料、药物递交到药物注册的全方位支持。自 2015 年起,我们已成功支持全球客户申报超过550 余项 IND、CTA、BLA、MAA、NDA 及 EUA 申报,完成200 多个 Module 3 CMC 申报件。
法规事务
依托深厚的法规专业积淀,我们为客户提供从 CMC 申报资料、药物递交到药物注册的全方位支持。自 2015 年起,我们已成功支持全球客户申报超过550 余项 IND、CTA、BLA、MAA、NDA 及 EUA 申报,完成200 多个 Module 3 CMC 申报件。
- 技术平台
- 发现
$药明生物提供了先进全面的抗体发现服务,用于创新型抗体的发现、鉴定和筛选提供全方位的服务。

- 返回
- WuXiBody ® 双特异性抗体平台
$WuXiBody ® 平台是药明生物开发的一个创新的、专有的技术平台,用于扩大双特异性抗体应用范围。基于最新的工程设计,该平台可以加快6-18个月的研发进程,大幅度降低产品的成本。
WuXiBody ® 双特异性抗体平台
WuXiBody ® 平台是药明生物开发的一个创新的、专有的技术平台,用于扩大双特异性抗体应用范围。基于最新的工程设计,该平台可以加快6-18个月的研发进程,大幅度降低产品的成本。
- WuXiHYbrid™ 杂交瘤单克隆抗体研发平台
$WuXiHYbrid™ 是国内领先、世界一流杂交瘤抗体研发平台,突破性提高了抗体新药研发的质量和速度,已为国内外50+客户成功交付超过200个高质量的单克隆抗体研发项目。
WuXiHYbrid™ 杂交瘤单克隆抗体研发平台
WuXiHYbrid™ 是国内领先、世界一流杂交瘤抗体研发平台,突破性提高了抗体新药研发的质量和速度,已为国内外50+客户成功交付超过200个高质量的单克隆抗体研发项目。
- WuXiLiAb™ 噬菌体展示人抗体库
$全人天然抗体库选取60个健康供体, 总数大于6x10e9 的PBMC或CBMC, 每个供体都单独建库并系统QC,保证了文库的高质量和多样性。
- 开发
$前沿的生物工艺平台与技术,旨在以更快的速度、更高的效率和更具成本效益的方式,推动高质量生物制剂进入临床试验阶段。

- 返回
- WuXian™ 定制化蛋白生产服务
$依托药明生物行业领先的高通量高表达、纯化和分析技术,提供各类蛋白生产服务,其中包括抗体、双抗、酶和重组蛋白表达。
WuXian™ 定制化蛋白生产服务
依托药明生物行业领先的高通量高表达、纯化和分析技术,提供各类蛋白生产服务,其中包括抗体、双抗、酶和重组蛋白表达。
- WuXia™ 细胞株构建
$药明生物为多种生物治疗药物提供全面的哺乳动物细胞系开发服务,从客户提供的DNA或蛋白质序列开始,到交付出高产量、高产品质量且稳定的单克隆结束。
WuXia™ 细胞株构建
药明生物为多种生物治疗药物提供全面的哺乳动物细胞系开发服务,从客户提供的DNA或蛋白质序列开始,到交付出高产量、高产品质量且稳定的单克隆结束。
- WuXiUPTM 超高效连续细胞培养生产平台
$WuXiUPTM 平台是强化型的灌流工艺,提供高产量,高质量的新一代生物药制造解决方案,灵活性高,成本低。
WuXiUPTM 超高效连续细胞培养生产平台
WuXiUPTM 平台是强化型的灌流工艺,提供高产量,高质量的新一代生物药制造解决方案,灵活性高,成本低。
- WuXiDARx™偶联技术平台
$药明合联研发了WuXiDARx™技术*,一种基于抗体天然半胱氨酸残基的偶联方式,为生物偶联药管线开发提供了更高的灵活性。
- 生产
$先进的生物制造平台赋能全球医疗合作伙伴,助力生物药快速迈向临床并成功上市,造福全球患者。
菜单
- 返回
- 一次性生物反应器
$我们运营着全球规模领先的数个一次性生物反应器生产基地。依托一次性使用系统在降低风险、生产灵活性、成本效益及环境友好性方面的卓越优势,为客户提供高效的生物药生产保障。
一次性生物反应器
我们运营着全球规模领先的数个一次性生物反应器生产基地。依托一次性使用系统在降低风险、生产灵活性、成本效益及环境友好性方面的卓越优势,为客户提供高效的生物药生产保障。
- Scale-Out生物药生产
$通过使用多个同等规模的反应器进行并联生产,我们能有效降低工艺放大风险,为您在临床至上市的各阶段提供极高的生产弹性,确保稳定供应。
Scale-Out生物药生产
通过使用多个同等规模的反应器进行并联生产,我们能有效降低工艺放大风险,为您在临床至上市的各阶段提供极高的生产弹性,确保稳定供应。
- 机器人无菌灌装
$我们采用全程序化、机器人自动化且无手套的隔离器技术,显著降低先进无菌制剂灌装过程中的生产风险。该系统具备极高的灵活性,能够支持各种复杂生物药及多样化包材系统的灌装需求。
机器人无菌灌装
我们采用全程序化、机器人自动化且无手套的隔离器技术,显著降低先进无菌制剂灌装过程中的生产风险。该系统具备极高的灵活性,能够支持各种复杂生物药及多样化包材系统的灌装需求。
- 连续细胞培养生产工艺
$结合强化灌流培养(IPC)与连续直接产物捕获(CDPC),并配备先进设备,实现生产效率提升并降低成本。
- Scale-Out生物药生产
- 可持续发展
- 职业发展
- 投资者
- 新闻与媒体
- WuXia™ 细胞株构建
- WuXiHYbrid™ 杂交瘤单克隆抗体研发平台
- 质量保证
- 分析检测
- 上下游工艺开发
- 开发
- 哺乳动物细胞
- 生产体系
